열역학 9장, 10장 동력 및 냉동 시스템
Updated:
열역학(Thermodynamics) 정리
열역학
• 제 1법칙: 에너지 보존
• 제 2법칙: 엔트로피 보존(가역 과정), 엔트로피 생성(비가역 과정)
• 물질의 상태량(property): 압력(P), 밀도($\rho$) 또는 비체적 (v), 온도(T), 내부에너지(u), 엔탈피(i), 엔트로피(s), 정압비열($C_p$), 정적비열($C_v$)
• 시스템(system), 경계(boundary), 주위(surrounding)
• 과정(process), 사이클(cycle), 압축성 물질(compressible substance)
열역학 총정리
(1) 질량보존: $\frac{dm}{dt} = \displaystyle\sum_{i} \dot{m_i} - \displaystyle\sum_{e} \dot{m_e}$
(2) 제 1법칙: $\frac{dE}{dt} = \frac{d}{dt} [m(u + \frac{V^2}{2} + g*z)] = \dot{Q} - \dot{W} + \displaystyle\sum_{i} \dot{m_i}(i_i + \frac{V_i ^2}{2} + g*z_i) - \displaystyle\sum_{e} \dot{m_e}(i_e + \frac{V_e ^2}{2} + g*z_e)$
(3) 제 2법칙: $\frac{dS}{dt} = \frac{\dot{Q}}{T} + \displaystyle\sum_{i} \dot{m_i}s_i - \displaystyle\sum_{e} \dot{m_e}s_e + \dot{S_{gen}}$ , $\frac{dS}{dt} \ge \frac{\dot{Q}}{T} + \displaystyle\sum_{i} \dot{m_i}s_i - \displaystyle\sum_{e} \dot{m_e}s_e$
동력 시스템
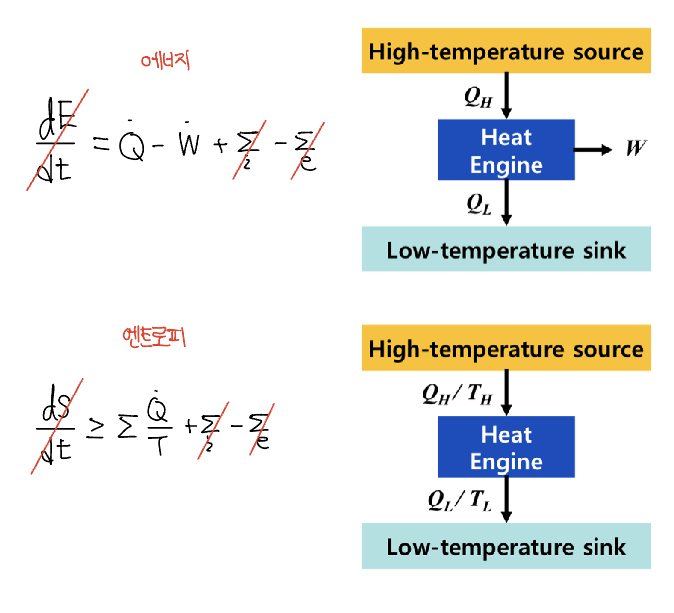
• 에너지 균형 (제 1법칙)
• 엔트로피 균형 (제 2법칙)
• 열효율 (복합법칙)
• 종류
(1) 상변화 사이클: Rankine
(2) 기체 사이클: Brayton, Stirling, Otto, 디젤
• 최대 동력
• 엔트로피 생성
• 비가역성(Irreversibility)
여기서, 엔트로피 생성은 각 부품별 생성 합이다.
Rankine 사이클
Rankine 사이클은 단순 증기 동력 발전소에 대한 적절한 모델이다. 각 상태와 과정을 다음과 같은 $T$-$s$선도상에 표시하면 편리하다.
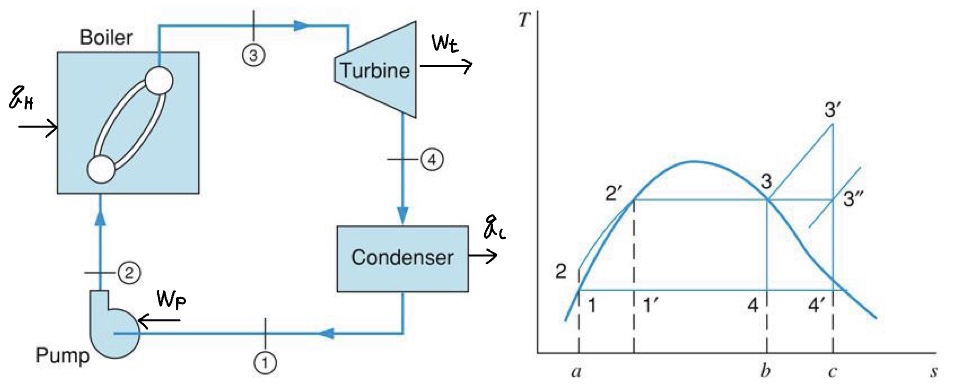
사이클은 다음의 네 과정으로 구성된다.
- 1-2: 펌프에서의 가역 단열 가압 $\mathrm{w}_P = i_2 - i_1 = \int_1^2 \mathrm{v}dP \approx \mathrm{v}_1(p_2 - p_1)$
- 2-3: 보일러에서의 등압 열전달 $q_H = i_3 - i_2$
- 3-4: 터빈에서의 가역 단열 팽창(또는 증기 기관과 같은 동력 생성 기기) $\mathrm{w}_t = i_3 -i_4$
- 4-1: 응축기에서의 등압 열전달 $q_L = i_4 - i_1$
응축기 출구 유동인 상태 1은 특별한 언급이 없는 한 포화 액체로 가정하여, $x_1 = 0$이다. 보일러 출구인 상태 3은 포화증기이지만, 많은 실제 시스템에서 보일러의 과열기를 통과하여 상태 $3^{\prime}$로 배출된다. 과열은 터빈 저압부의 건도를 상태 4에서 상태 $4^{\prime}$로 증가시키는 효과가 있다.
Rankine 사이클은 네 개 부품을 각각 검사체적으로 잡아 해석한다. 사이클에서 에너지 전달은 부호에 특히 주의해야 하는데, 모든 $q$와 w를 그림에 나타낸 방향을 양(+)으로 선택한다.
열전달과 $T$-$s$선도 면적의 관계를 살펴보자. 보일러에서 가한 $q$는 곡선 $2-2^{\prime}-3$하부 면적이고, 응축기에서 나간 열 $q_L$은 곡성 $4-1$하부 면적이다. 두 열전달의 차이가 순수 열전달인데, 이 값이 순수 일과 같으므로, 면적으로 사이클 효율을 나타낼 수 있다.
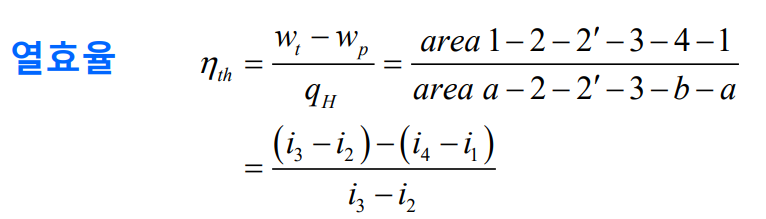
Rankine 사이클의 변환 효율은 동일한 조건의 Carnot 사이클보다 명백히 낮다. 그 이유는 $2-2^{\prime}$부분으로 인해 가열 과정의 평균 온도가 더 낮기 때문이다. 일정한 고압과 일정한 저압의 Carnot 사이클은 그림 $1^{\prime}-2^{\prime}-3-4-1^{\prime}$로 나타낼 수 있다. 펌프는 2상 혼합물을 가압해야 하고, 터빈은 저압부에서 매우 낮은 건도를 갖게 된다. 만일 등온 과정으로 $3^{\prime\prime}$까지 과열한다면 과열증기 영역에서 압력이 감소해야 하므로, 열전달이 있는 터빈이 필요하다. 이런 모든 과정은 가능하지 않거나 효율이 지나치게 낮게 된다. Rankine 사이클은 구현은 가능한 이상적인 사이클에 가까우며, 부분적인 개조를 통해 기본 사이클보다 효율을 높일 수 있다.
다음 예제들을 보자.
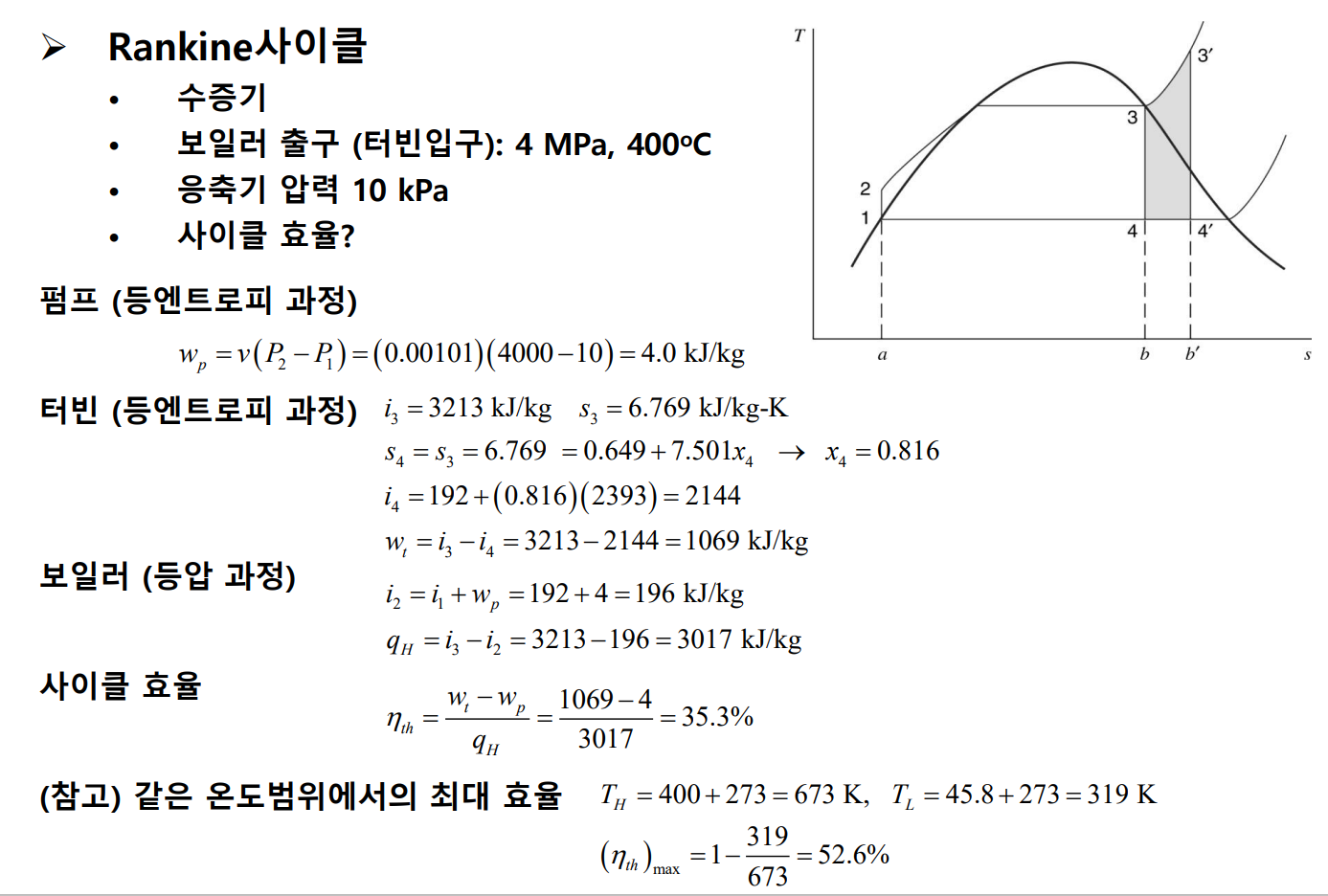


재열 사이클
열을 공급하는 동안의 압력이 증가하면 Rankine 사이클의 효율이 증가하지만 압력이 증가하면 터빈의 저압 출구에서 수증기의 습분이 증가한다. 재열 사이클(reheat cycle)은 압력을 증가시켜 사이클의 효율을 높이는 동시에 터빈의 저압 출구에서 습분이 너무 증가하지 않도록 고안된 사이클이다. 이 사이클에 대한 구성과 $T$-$s$ 선도는 다음과 같다.
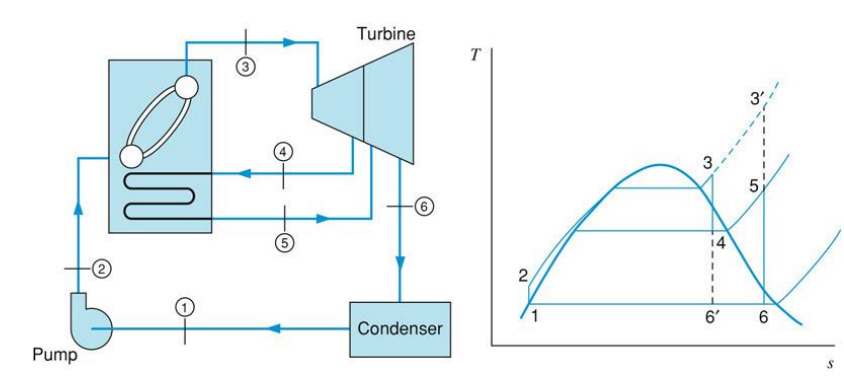
수증기는 터빈에서 중간 정도의 압력까지만 팽창하고 보일러에서 재열된 후 다시 터빈으로 토출 압력까지 팽창한다. $T$-$s$선도에서 알 수 있듯이, 수증기의 재열로 인해 열을 공급하는 평균 온도는 크게 변화하지 않으므로 사이클의 효율 증가도 크지 않다. 이 사이클의 주된 장점은 터빈의 저압부에서 습분을 안전한 값까지 낮추는 데 있다. 증기를 $3^{\prime}$까지 과열할 수 있는 금속이 있다면, 단순 Rankine 사이클이 재열 사이클보다 더 효율적이며 재열 사이클은 필요하지 않을 것이다.
재생 사이클
Rankine 사이클의 또 다른 중요한 변형은 급수 가열기(feedwater heater)를 사용하는 재생 사이클(regenerative cycle)이다. 다음과 같은 현실적인 재생 사이클을 생각해 보자.
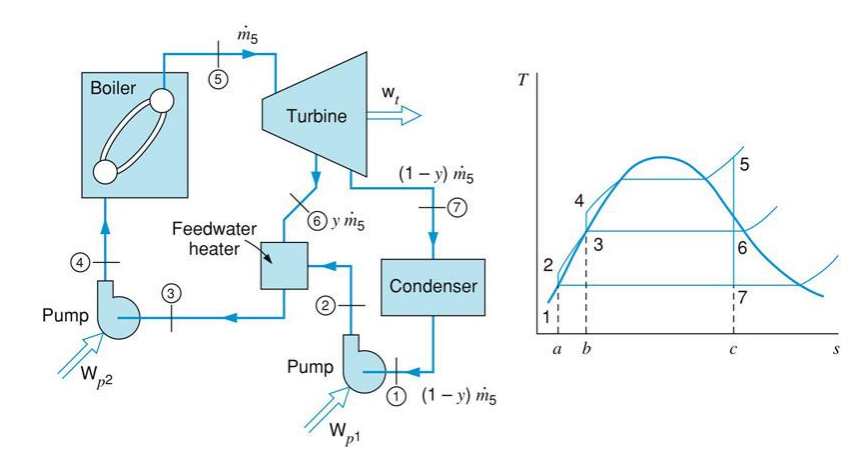
위 사이클에서는 터빈에서 일부 팽창된 증기의 일부를 추출하여 급수 가열기에 공급한다.
수증기는 상태 5로 터빈에 들어간다. 상태 6까지 팽창된 후, 수증기의 일부는 추출되어 급수 가열기에 공급된다. 남은 수증기는 터빈에서 상태 7까지 팽창하고 응축기에서 응축된다. 응축된 액체는 펌프를 통해 급수 가열기로 보내지고, 여기서 터빈에서 추출된 수증기와 혼합된다. 추출되는 수증기의 비율은 급수 가열기 출구의 액체가 상태 3의 포화 액체가 되도록 결정한다. 액체는 보일러 압력까지 가압하지 않고 상태 6에 해당되는 중간 압력까지만 가압한다. 따라서 또 다른 펌프를 이용하여 급수 가열기의 출구 액체를 보일러 압력까지 가압한다. 여기서 중요한 점은 열을 공급하는 동안의 평균 온도가 증가했고 열기관의 효율이 크게 증가했다.
터빈 효율

펌프 효율

압축기 효율

Brayton 사이클
작동 유체가 응축되는 경우를 Rankine 사이클이라 하고, 작동 유체가 항상 단상의 기체인 경우를 Brayton 사이클이라 한다. 공기 표준 Brayton 사이클은 단순 가스 터빈(gas turbine)의 이상 사이클이다. 내연 과정을 이용하는 단순 개방 사이클 가스 터빈과 열전달 과정을 이용하는 단순 밀폐 사이클 가스 터빈은 다음과 같다.
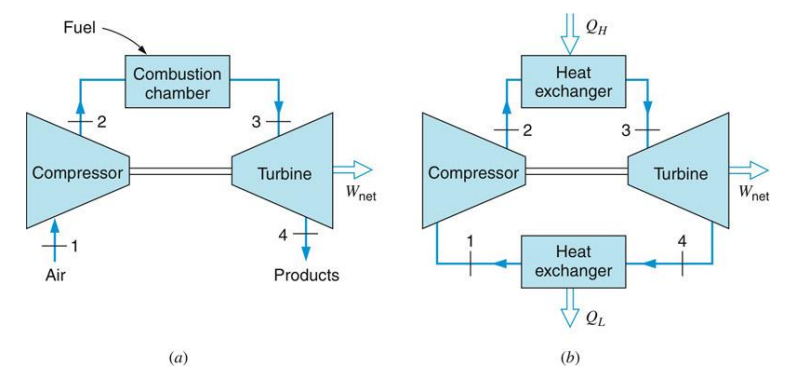
공기 표준 Brayton 사이클의 $T$-$s$선도는 다음과 같다.
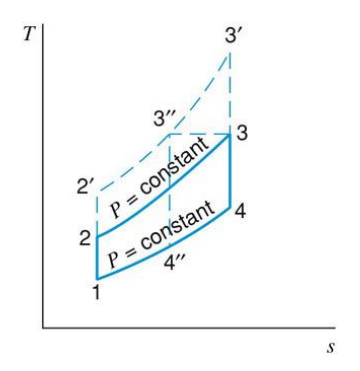
사이클은 다음의 네 과정으로 구성된다.
- 1-2: 압축기에서의 등엔트로피 과정 $\mathrm{w}_c = i_2 - i_1$
- 2-3: 가열기에서의 등압 열전달 $q_H = i_3 - i_2$
- 3-4: 터빈에서의 등엔트로피 과정 $\mathrm{w}_T = i_3 - i_4$
- 4-1: 냉각기에서의 등압 열전달 $q_L = i_4 - i_1$
Brayton 사이클은 위 그림의 (b)의 네 부품을 각각 검사 체적으로 잡아 해석할 수 있는다. 사이클의 효율은 다음과 같다.

공기 표준 Brayton 사이클의 효율은 등엔트로피 압력비의 함수이다. 효율은 압력비에 따라 증가한다. 이는 압력비가 증가하면 사이클이 $1-2-3-4-1$에서 $1-2^{\prime}-3^{\prime}-4-1$로 변화하기 때문이다. 두 경우 방출하는 열은 같으나 후자의 경우 전자보다 공급하는 열이 더 많으므로 효율이 더 높게 된다. 후자의 경우 최고 온도가 $T_3^{\prime}$으로 전자의 $T_3$보다 높다. 실제 가스 터비에서 기체의 터빈 입구 최고 온도는 터빈의 재료에 따라 제한된다. 따라서 온도 $T_3$를 고정시키고 압력비를 증가시키면, 사이클은 $1-2^{\prime}-3^{\prime\prime}-4^{\prime\prime}-1$로 변화한다.
재생기가 있는 단순 가스 터빈 사이클
가스 터빈 사이클의 효율은 재생기를 도입하여 향상시킬 수 있다. 재생기가 있는 단순 개방 가스 터빈 사이클의 구성은 다음과 같고, 이에 대응하는 공기 표준 이상 사이클의 $T$-$s$선도를 나타내었다.
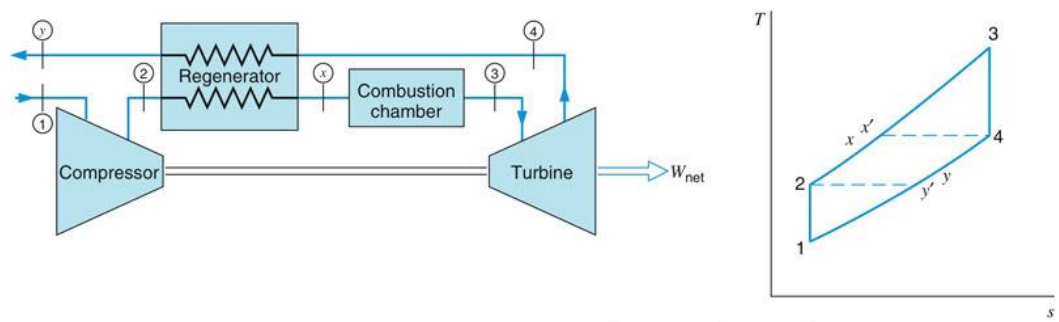
사이클 $1-2-x-3-4-y-1$에서 터빈 출구인 상태 4의 기체(배기 가스)온도는 압축기 출구의 기체 온도보다 높다. 따라서 배기 가스에서 압축기 출구의 고압 기체로 열이 전달될 수 있다. 재생기의 한 가지인 대향류 열교환기(counterflow heat exchanger)를 사용할 때, 이상적으로는 재생기 출구에서 고압 기체의 온도 $T_x$가 터빈 출구의 기체 온도 $T_4$와 같게 된다. 외부 열원으로부터의 열전달은 기체의 온도를 $T_x$에서 $T_3$까지 증가시키는 데에만 필요하다.
압축기와 터빈에 있어서 단열 과정보다 등온 과정이 더 유리하다. 두 개의 가역 등압 과정과 두 개의 등온 과정으로 구성된 사이클을 Ericsson 사이클이라 한다. Brayton 가스 터빈 사이클을 수정하여 Ericcson 사이클의 성능에 가깝도록 하는 방법이 있다. 이 방법은 중간 냉각(intercooling)을 하는 다단 압축(multi-stage compression)과 재열을 하는 다단 팽창(multi-stage expansion)으로 이루어진다. 2단 압축과 2단 팽창을 하고 재생기를 부착한 공기 표준 사이클의 구성은 다음과 같다.
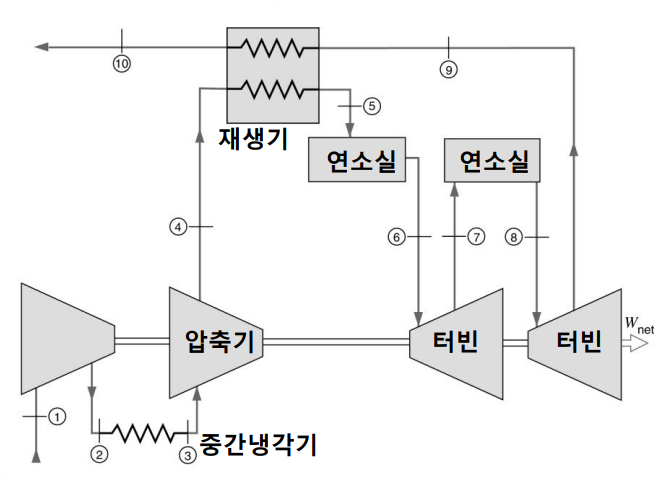
이상적인 사이클에서 중간 냉각기 출구의 공기 온도는 1단 압축기 입구의 공기 온도과 같고, 재열기 출구의 공기온도는 제1터빈 입구의 공기온도와 같다. 또한 이상적인 사이클에서 재생기 출구의 고압 기체 온도는 터빈 출구의 저압 공기 온도와 같다.
냉동 시스템
• 에너지 균형 (제 1법칙)
• 엔트로피 균형 (제 2법칙)
• 성능계수 (복합법칙)
• 종류
(1) 상변화 사이클: 증기압축, 흡수식
(2) 기체 사이클: 역Brayton, 역Stirling
(3) 열전(thermoelectric) 사이클
• 최소 동력
• 엔트로피 생성
• 비가역성(Irreversibility)
여기서, 엔트로피 생성은 각 부품별 생성 합이다.
증기 압축 냉동 사이클
사이클 동안 상변화를 하는 작동 유체에 대한 이상적인 냉동 사이클을 살펴보자. 다음은 증기 압축 냉동(vapor compression refrigeration)시스템의 이상 모델이다.
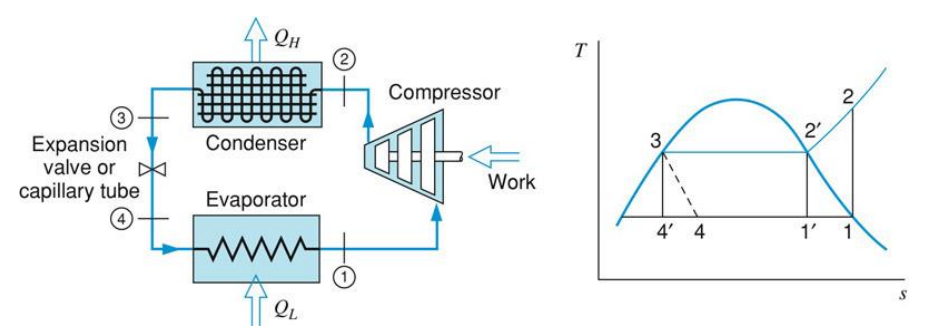
사이클은 다음의 네 과정으로 구성된다.
- 1-2: 압축기에서 저압의 포화 증기를 고압으로 가역 단열 압축, 등앤트로피 과정 $\mathrm{w}_c = i_2 - i_1$
- 2-3: 응축기에서 등압으로 열이 방출되며 작동 유체는 포화 액체로 응축 $q_H = i_2 - i_3$
- 3-4: 팽창밸브에서 고압의 액체가 팽창하며 저압의 포화상태가 되는 단열 스로틀 과정, 등엔탈피, 등엔트로피 과정 $i_3 = i_4$
- 4-1: 증발기에서 포화 냉매가 외부에서 열을 흡수하여 증발(냉동)하는 등압 증발 과정 $q_L = i_1 - i_4$
이 사이클은 Rankine 사이클의 역사이클과 유사하다. 이 사이클과 작동 유체가 항상 2상 영역에 있는 $1^{\prime}-2^{\prime}-3-4^{\prime}-1^{\prime}$의 Carnot 사이클과의 차이점을 살펴보자. Carnot 사이클의 과정 $1^{\prime}-2^{\prime}$에서와 같이 액체와 증기의 혼합물이 압축하기보다는 증기만을 압축하기가 훨씬 용이하다. 적절한 속도로 상태 $1^{\prime}$과 같은 혼합물을 압축하면서 액체와 증기 간의 평형을 유지하는 것은 사실상 불가능하다.
이상적인 사이클에 하나의 비가역 부품인 스로틀 밸브는 두 가지 용도 중 하나로 사용된다. 첫번째 용도는 냉동 시스템인데, 주어진 공간을 주변 온도인 $T_3$보다 낮은 저온 $T_1$으로 유지한다. 따라서 이 경우에 설정된 시스템 목표는 $q_L$이고, 냉동 시스템 성능은 성능계수로 나타낸다.
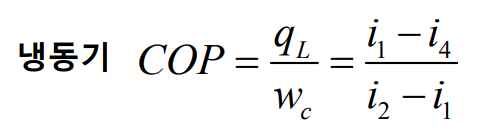
두 번째 용도는 열펌프(heat pump)시스템인데, 이 경우 일정한 공간을 주변(또는 열원) 온도 $T_1$보다 높은 온도 $T_3$로 유지하고자 한다. 시스템을 사용하는 목적은 $q_H$를 얻는데 열펌프의 성능 계수는 다음과 같다.
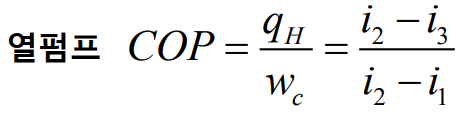
다음 예제들을 보자.



흡수식 냉동 사이클
흡수식 냉동 사이클(absorption refrigeration cycle)은 압축하는 방법이 증기 압축 사이클과 다르다. 흡수식 사이클에서 저압의 증기는 물에 흡수되어 수용액이 되고, 수용액은 액체 펌프에 의해 고압으로 가압된다. 다음은 이러한 시스템의 기본 요소의 구성을 나타내고 있다.
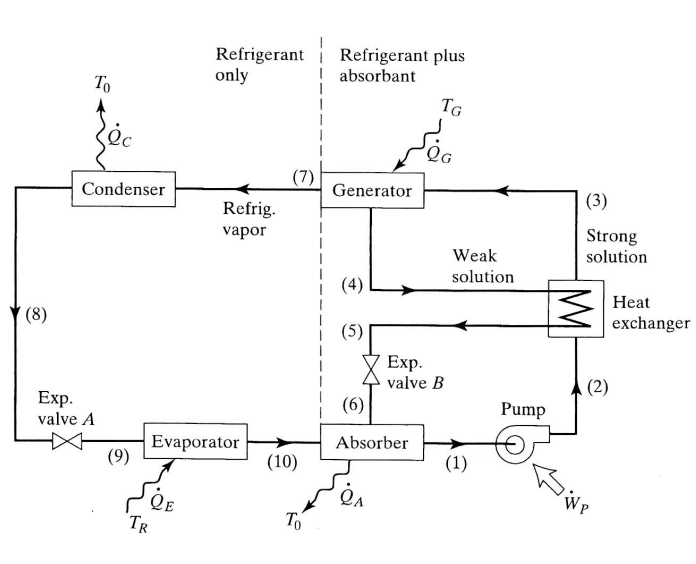
저압의 암모니아 증기는 증발기(evaporator)를 떠나 흡수기(absorber)에 유입되고 여기서 묽은 암모니아 용액(weak solution)에 흡수된다. 이 과정은 주위보다 약간 높은 온도에서 진행된다. 이 과정 동안 열은 주위로 방출되어야 한다. 짙은 암모니아 용액(strong solution)은 가압되어 열교환기를 지나 발생기(generator)로 가며, 발생기는 고온과 고압으로 유지된다. 이러한 조건하에서 고온의 열원으로부터 열이 전달되면 암모니아 증기가 용액에서 추출된다. 이 암모니아 증기는 응축기(condenser)로 가서 응축된 후, 팽창 밸브를 거쳐 증발기로 보내진다. 묽은 암모니아 용액은 열교환기를 지나 흡수기로 되돌아간다.
흡수식 시스템에서는 액체를 가압하기 때문에 필요한 입력일이 매우 작은 장점이 있다. 운동 에너지와 위치 에너지의 변화가 없는 가역 정상상태 과정에서 일은 $-\int \mathrm{v} \, dP$인데, 액체의 비체적이 증기의 비체적보다 매우 작기 때문이다. 반면에 대체로 고온의 열원이 필요하다.
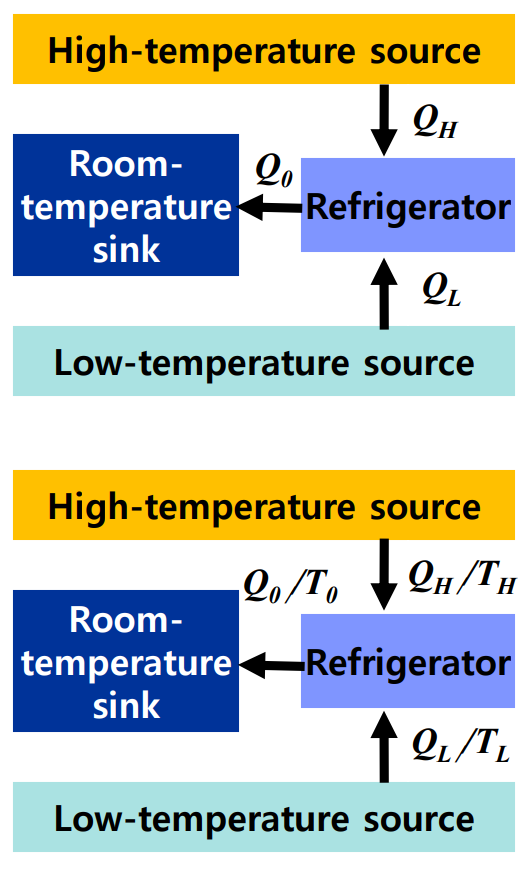
열구동 냉동시스템
• 에너지 균형 (제 1법칙)
• 엔트로피 균형 (제 2법칙)
• 성능계수 (복합법칙)
• 종류
(1) 흡수식 냉동시스템
(2) 열기관 + 증기압축 냉동시스템
(3) VM사이클 냉동시스템
냉매
증기 압축 냉동 시스템에서는 증기 동력 사이클보다 훨씬 많은 종류의 작동 유체(냉매)를 사용한다. 증기 압축 냉동의 초기에는 암모니아와 이산화항이 중요한 냉매였으나, 두 가지 모두 유독하며 위험한 물질이다. 근래에는 보통 CFC(chloro-fluoro-carbon)로 불리는 냉매를 사용한다. 이러한 종휴의 냉매는 상온에서 화학적으로 대단히 안정하며, 특히 수소 원자가 없는 경우 더욱 안정하다. 이러한 특성은 작동 유체인 냉매에 꼭 필요하다. 반면에 이러한 특성은 치명적인 결과를 초래할 수도 있는데 이는 기체가 냉동 기기에서 대기 중으로 유출되면 수년에 걸쳐 성층권으로 서서히 확산되어가기 때문이다. 성층권에서 냉매는 분해되어 염소를 배출하여 오존층을 파괴한다. 따라서 이미 널리 사용되고 있으나 생태계를 위협할 수 있는 CFC를 제거하고 적정한 대체물을 개발하는 일은 대단히 중요하게 되었다. 대체 냉매들은 HFC계 냉매(R-134a, R-152a), 천연 냉매(암모니아, 이산화탄소, 물)등이 있다.
댓글남기기